A partir de los 40 años, muchas personas —especialmente mujeres— notan un fenómeno frustrante: la grasa se acumula con mayor facilidad en el abdomen, incluso manteniendo hábitos similares a los de años anteriores. No es solo una cuestión de calorías o de fuerza de voluntad. Detrás de este cambio hay una interacción compleja entre hormonas, metabolismo y sistema nervioso, donde la resistencia a la insulina y el cortisol juegan un papel central.
En este artículo vamos a desentrañar, desde la fisiología y la bioquímica, por qué ocurre, qué mecanismos están implicados y, sobre todo, qué podemos hacer para revertir o mejorar esta situación.
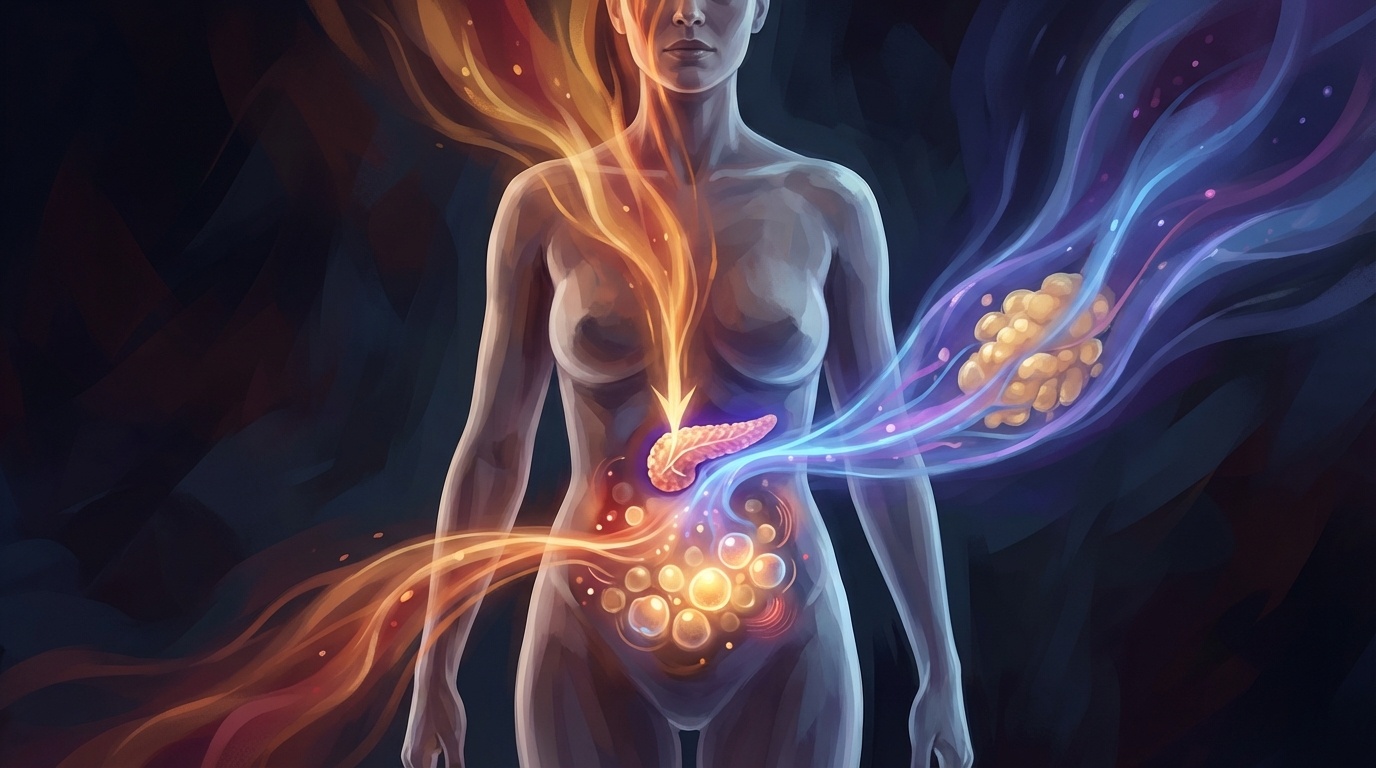
Lo primero que tenemos que tener en cuenta es el abdomen como un tejido metabólicamente activo. En este caso, el tejido adiposo abdominal, especialmente el tejido adiposo visceral, no es un simple “depósito de grasa”. Es un órgano endocrino activo, altamente sensible a señales hormonales como: Insulina, Cortisol, Estrógenos y progesterona y Catecolaminas (adrenalina y noradrenalina).
Con el paso de los años, este tejido se vuelve más reactivo al estrés y menos eficiente en el manejo de la glucosa, lo que crea el escenario perfecto para la acumulación de grasa central.
Resistencia a la insulina: el punto de partida metabólico
¿Qué es realmente la resistencia a la insulina?
La insulina es la hormona encargada de facilitar la entrada de glucosa en las células, principalmente en músculo, hígado y tejido adiposo. Cuando estas células dejan de responder adecuadamente, el páncreas compensa produciendo más insulina. Este estado de hiperinsulinemia crónica tiene varias consecuencias claves:
- Favorece el almacenamiento de grasa
- Inhibe la lipólisis (quema de grasa)
- Estimula la adipogénesis abdominal
- Aumenta la inflamación de bajo grado
¿Por qué aumenta después de los 40 esta resistencia a la insulina?
Esto se debe porque a partir de esta edad confluyen varios factores:
- Disminución de masa muscular (también llamada sarcopenia)
- Menor actividad de GLUT-4 en músculo
- Cambios hormonales (ya sea en la perimenopausia / andropausia)
- Mayor exposición al estrés crónico
- Alteraciones del sueño
El resultado es una menor capacidad de manejar los picos de glucosa, incluso con dietas aparentemente “normales”.
Cortisol: la hormona del estrés que cambia el metabolismo
Debemos tener en cuenta que el cortisol es una hormona esencial para la vida. El problema no es su presencia, sino su elevación crónica. ¿Qué hace el cortisol a nivel metabólico?
Desde la fisiología: aumenta la gluconeogénesis hepática, eleva la glucosa en sangre, antagoniza la acción de la insulina y promueve la lipogénesis visceral. Hay que destacar que el tejido adiposo abdominal tiene alta densidad de receptores de cortisol, lo que explica por qué el estrés se traduce tan fácilmente en grasa central.
Estrés moderno y cortisol persistente
Después de los 40, muchas personas viven una combinación de estrés laboral sostenido, responsabilidades familiares, falta de descanso real y en algunos casos entrenamiento excesivo o mal programado. Todo esto mantiene al eje hipotálamo–hipófisis–adrenal (HHA) activado de forma constante, favoreciendo un estado metabólico ahorrador y proinflamatorio.
Y es aquí cuando hablamos de una sinergia peligrosa: cortisol + insulina
Aquí se encuentra uno de los núcleos fisiológicos más relevantes —y menos comprendidos— del aumento de grasa abdominal después de los 40: la interacción bidireccional entre cortisol e insulina. No actúan de forma aislada, sino que se refuerzan mutuamente creando un entorno metabólico claramente desfavorable.
Cuando el cortisol se eleva de forma crónica, estimula la producción hepática de glucosa mediante gluconeogénesis. Este aumento sostenido de glucosa obliga al páncreas a secretar más insulina para mantener la homeostasis. Sin embargo, en un contexto de resistencia a la insulina, esta respuesta es cada vez menos eficaz, por lo que la insulina permanece elevada durante más tiempo. El organismo interpreta este escenario como una situación de amenaza energética y prioriza el almacenamiento, especialmente en el tejido adiposo visceral, que presenta una alta densidad tanto de receptores de insulina como de glucucorticoides.
A su vez, la hiperinsulinemia reduce la capacidad del organismo para movilizar grasa (inhibe la lipólisis) y potencia la acción lipogénica del cortisol en el abdomen. Este círculo vicioso explica por qué dietas muy restrictivas, entrenamientos excesivos o ayunos mal planteados pueden empeorar el problema: más estrés fisiológico implica más cortisol, más glucosa circulante y, paradójicamente, más grasa abdominal. El cuerpo no “se resiste a adelgazar”; se está protegiendo desde la biología.
Cambios hormonales después de los 40 y su impacto
En el caso particular de las mujeres, la transición a la perimenopausia implica:
- Fluctuaciones de estrógenos
- Menor efecto protector sobre la sensibilidad a la insulina
- Mayor activación del eje del estrés
Los estrógenos tienen un efecto insulinosensibilizante y antiinflamatorio. Su descenso relativo favorece:
- Redistribución de grasa hacia el abdomen
- Mayor resistencia a la insulina
- Mayor respuesta al cortisol
Inflamación de bajo grado: el terreno metabólico
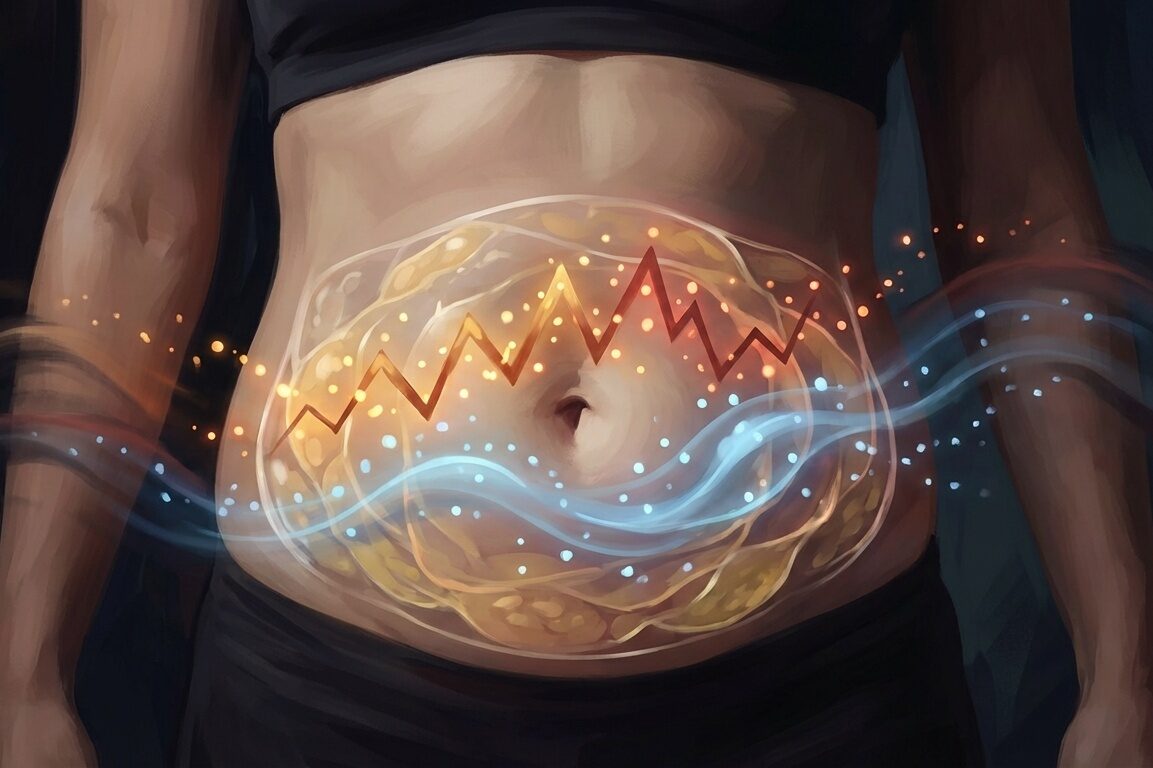
La grasa abdominal no es metabólicamente neutra. Cuando se expande, especialmente a nivel visceral, se convierte en un foco activo de inflamación crónica de bajo grado, un estado silencioso pero persistente que altera profundamente la fisiología metabólica.
Los adipocitos hipertrofiados y el tejido adiposo infiltrado por macrófagos comienzan a secretar citocinas proinflamatorias como TNF-α, IL-6 y MCP-1, además de adipocinas disfuncionales como la resistina. Estas moléculas interfieren directamente con la señalización de la insulina a nivel celular, bloqueando la vía del receptor de insulina y del IRS-1, lo que agrava aún más la resistencia a la insulina. Al mismo tiempo, esta inflamación altera la función mitocondrial, incrementa el estrés oxidativo y afecta al metabolismo hepático de lípidos y glucosa.
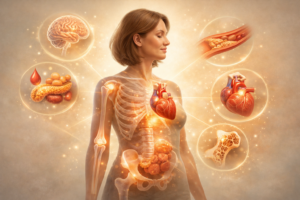
Desde una perspectiva narrativa, podemos entender la inflamación de bajo grado como un “ruido metabólico constante”. No genera síntomas agudos claros, pero mantiene al organismo en un estado de alerta permanente. Este contexto inflamatorio estimula el eje hipotálamo–hipófisis–adrenal, perpetuando la liberación de cortisol, cerrando así el círculo entre estrés, inflamación y disfunción metabólica. Con el paso del tiempo, este terreno favorece no solo la acumulación de grasa abdominal, sino también el desarrollo de patologías como síndrome metabólico, diabetes tipo 2, enfermedad cardiovascular y envejecimiento acelerado.
¿Qué podemos hacer desde la fisiología?
1. Mejorar la sensibilidad a la insulina: Priorizar proteína suficiente
- Controlar la carga glucémica, no solo las calorías
- Entrenamiento de fuerza regular
- Evitar picos frecuentes de glucosa
2. Modular el cortisol
- Dormir 7–8 horas reales
- Evitar ayunos extremos bajo estrés
- Reducir cardio crónico de alta intensidad
- Introducir técnicas de respiración y recuperación
3. Proteger la masa muscular
El músculo es el principal destino de la glucosa. Mantenerlo activo y funcional es clave para revertir la resistencia a la insulina.
La grasa abdominal después de los 40 no es un fallo personal, es una señal fisiológica. Entender la interacción entre resistencia a la insulina, cortisol y cambios hormonales nos permite dejar de luchar contra el cuerpo y empezar a trabajar con él. Cuando se aborda desde la fisiología —y no desde la restricción— el metabolismo puede volver a responder.
Porque a esta edad, no se trata de comer menos, sino de regular mejor.
Referencias científicas
- Reaven, G. M. (1988). Role of insulin resistance in human disease. Diabetes, 37(12), 1595–1607.
- Kahn, B. B., & Flier, J. S. (2000). Obesity and insulin resistance. Journal of Clinical Investigation, 106(4), 473–481.
- Rosmond, R. (2005). Role of stress in the pathogenesis of the metabolic syndrome. Psychoneuroendocrinology, 30(1), 1–10.
- Bjorntorp, P. (2001). Do stress reactions cause abdominal obesity and comorbidities? Obesity Reviews, 2(2), 73–86.
- Hotamisligil, G. S. (2006). Inflammation and metabolic disorders. Nature, 444(7121), 860–867.
- Shoelson, S. E., Lee, J., & Goldfine, A. B. (2006). Inflammation and insulin resistance. Journal of Clinical Investigation, 116(7), 1793–1801.
- Pasquali, R., et al. (2006). Stress, obesity and metabolic syndrome. Annals of the New York Academy of Sciences, 1083, 111–128.